mRNA疫苗的体外稳定性
正如之前在背景介绍中提到的,目前已批准的 mRNA疫苗流通的主要障碍之一是它们必须以冷冻形式储存。在 2–8 °C 的温度下,辉瑞/BioNTech 和 Moderna 疫苗分别可稳定保存 5 天和 30 天,两家公司都为终端使用提供了详细的处理说明。有趣的是,据报道 CureVac 的候选疫苗在冰箱温度和 -60 °C 下可稳定 3 个月。这些是目前发布了mRNA-LNP长期储存条件的制造商,这种苛刻的温度要求严重影响了这些疫苗的储存、运输和流通。然而,迄今为止,在公开资料中几乎没有关于优化mRNA 疫苗稳定性的信息。本节旨在概述影响 mRNA-LNP 疫苗成分稳定性的因素,并讨论分析评价这种稳定性的方法。
mRNA稳定性
强烈影响所需储存条件的主要因素是 mRNA 的稳定性。如上文2.1 节所述,mRNA 分子的结构经过专门设计可以用于增加体内靶抗原的翻译。mRNA 的特殊性在于,即使是长 mRNA 链(通常长度在 1000 到 5000 个核苷酸之间)中的一个核苷酸发生变化(链断裂或碱基氧化)便会导致翻译终止。这使得 mRNA 疫苗与其他疫苗完全不同,在其他疫苗中,抗原的微小变化不一定对其功效产生显影响。因此,对于 mRNA 疫苗,监测整个分子的完整性是至关重要的。
mRNA 降解的方式有多种,可以分为化学和物理降解。化学降解包括 mRNA 分子中化学键的改变。物理不稳定性包括变性(二级和三级结构的丧失),与变性对蛋白质生物制剂活性的影响不同,物理不稳定性对mRNA的影响可能不太明显。然而,变性还包括聚集和沉淀等变化,这些变化会影响mRNA的翻译表达。在一篇关于核酸稳定性的综述中,Pogocki 和 Sch?neich 指出化学降解在siRNA降解中的影响比物理不稳定性更大,对于链长更长的 mRNA来说可能更是如此。
mRNA在体外的化学降解主要包括水解和氧化,水解主要是发生在mRNA 分子骨架的磷酸二酯键(图5 )。核糖上的2' OH 基团起着至关重要的作用,因为导致 mRNA 链断裂的酯交换反应起始于磷酸酯键上的 2'OH 基团的亲核进攻导致 P-O5' 酯键断裂(图5)。这个过程需要水,可以被核酸酶催化,也可以被 mRNA 分子本身和其他外源因素如酸和碱催化。在有关 mRNA 水解的两篇文献中,作者指出 mRNA 的碱基序列和二级结构会影响水解速率。具体而言,碱基堆积可能会降低磷酸二酯键的裂解速率,可以小化 mRNA 分子的“平均未配对概率”。可以使用专门设计的算法来选择可以形成大双链区域的单链 mRNA 的核苷酸序列。据称,采用这种方法优化后,体外稳定性得到了改善。
CureVac、辉瑞/BioNTech 和 Moderna 疫苗之间的区别在于后两者具有 1-甲基-假尿苷的单核苷掺入。之前的一项研究表明,这种修饰提高了 RNA 二级结构的稳定性。CureVac 采用提高GC比例策略,具有类似的效果。
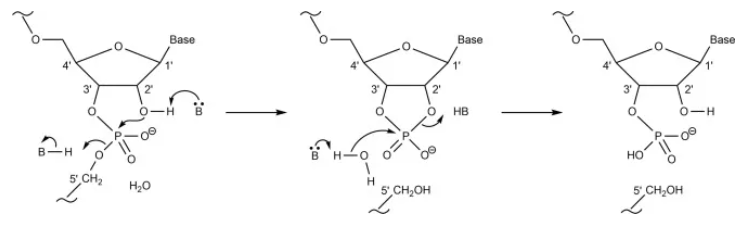
图5 通过 2',3'-环状磷酸酯,碱基催化RNA分子内的磷酸二酯键水解、B表示Br?nsted碱。
相反,氧化会影响碱基,并在较小程度上影响mRNA 核糖单位的糖基团。氧化可导致碱基裂解、链断裂和 mRNA 二级结构的改变。然而,如前所述,水解似乎被认为是驱动 mRNA 降解的关键因素。
原文文献:
Linde,S;Dominik ,W;Jayesh A. K;Rein ,V;Gideon ,K;Wim ,J;Daan J.A. C.mRNA-lipid nanoparticle COVID-19 vaccines: Structure and stability.International Journal of Pharmaceutics.2021,601,120586
参考文献来源:
1. Abdelwahed, W., Degobert, G., Stainmesse, S., Fessi, H., 2006. Freeze-drying ofnanoparticles: Formulation, process and storage considerations. Adv. Drug Deliv.Rev. 58 (15), 1688–1713. https://doi.org/10.1016/j.addr.2006.09.017.
2. Yanez Arteta, M., Kjellman, T., Bartesaghi, S., Wallin, S., Wu, X., Kvist, A.J.,Dabkowska, A., Sz′ekely, N., Radulescu, A., Bergenholtz, J., Lindfors, L., 2018. Successful reprogramming of cellular protein production through mRNA delivered
by functionalized lipid nanoparticles. Proc. Natl. Acad. Sci. U. S. A. 115 (15),E3351–E3360. https://doi.org/10.1073/pnas.1720542115.
3. Ayat, N.R., Sun, Z., Sun, D.a., Yin, M., Hall, R.C., Vaidya, A.M., Liu, X., Schilb, A.L.,Scheidt, J.H., Lu, Z.-R., 2019. Formulation of biocompatible targeted ECO/siRNAnanoparticles with long-term stability for clinical translation of RNAi. Nucleic AcidTher. 29 (4), 195–207. https://doi.org/10.1089/nat.2019.0784.
4. Baden, L.R., El Sahly, H.M., Essink, B., Kotloff, K., Frey, S., Novak, R., Diemert, D.,Spector, S.A., Rouphael, N., Creech, C.B., McGettigan, J., Khetan, S., Segall, N.,Solis, J., Brosz, A., Fierro, C., Schwartz, H., Neuzil, K., Corey, L., Gilbert, P.,Janes, H., Follmann, D., Marovich, M., Mascola, J., Polakowski, L., Ledgerwood, J.,Graham, B.S., Bennett, H., Pajon, R., Knightly, C., Leav, B., Deng, W., Zhou, H.,Han, S., Ivarsson, M., Miller, J., Zaks, T., 2021. Efficacy and safety of the mRNA-1273 SARS-CoV-2 vaccine. N. Engl. J. Med. 384 (5), 403–416. https://doi.org/10.1056/NEJMoa2035389.
5. Ball, R.L., Bajaj, P., Whitehead, K.A., 2016. Achieving long-term stability of lipidnanoparticles: examining the effect of pH, temperature, and lyophilization. Int. J.Nanomed. 12, 305–315. https://doi.org/10.2147/IJN.S123062.
6. Bloom, K., van den Berg, F., Arbuthnot, P., 2020. Self-amplifying RNA vaccines forinfectious diseases. Gene Ther. 1–13 https://doi.org/10.1038/s41434-020-00204-y.Brader, M.L., Williams, S.J., Banks, J.M., Hui, W.H., Zhou, Z.H., Jin, L., 2021.
7. Encapsulation state of messenger RNA inside lipid nanoparticles. Biophys. J. https://doi.org/10.1016/j.bpj.2021.03.012.
8. Brisco, M.J., Morley, A.A., 2012. Quantification of RNA integrity and its use formeasurement of transcript number. e144–e144 Nucleic Acids Res. 40. https://doi.
org/10.1093/nar/gks588.
9.Burke, P.A., Gindy, M.E., Mathre, D.J., Kumar, V., Prud’homme, R.K., 2013. Preparationof Lipid Nanoparticles. US 2013/0037977.
10. Buschmann, M.D., Carrasco, M.J., Alishetty, S., Paige, M., Alameh, M.G., Weissman, D.,2021. Nanomaterial delivery systems for mRNA vaccines. Vaccines 9 (1), 65. https://doi.org/10.3390/vaccines9010065.