新冠疫情的爆发与持续流行给全球造成了重大影响,但同时,也让我们见证了mRNA技术的巨大潜力。
稳定性是mRNA疫苗开发中面临的主要挑战之一,目前已上市的两款mRNA疫苗均需要在严格低温下保存和运输,这无疑增加了疫苗的保存和运输的难度和成本,显著限制了疫苗的大规模推广普及。
将制剂制成冻干剂型是提升其稳定性最常用方法之一。目前,国内外均有冻干剂型mRNA疫苗已进入到临床阶段。
1.国产全球首款冻干剂型新冠奥密克戎株mRNA疫苗RH109进入临床阶段
6月27日,深圳市瑞吉生物科技有限公司(以下简称“瑞吉生物”)宣布,其研发的冻干新型冠状病毒奥密克戎株mRNA疫苗RH109由下设合资公司(武汉瑞科吉生物科技有限公司)分别在新西兰和菲律宾获得临床批件。本次获批,标志着全球首款冻干型新冠奥密克戎株mRNA疫苗进入临床阶段。
RH109采用瑞吉生物自行开发的冻干技术,可以有效地维持mRNA-LNP的理化性质和生物活性,并能在2至8℃的温度下实现长期储存。
2.Moderna巨细胞病毒(CMV)疫苗mRNA-1647III期临床预计23年1月完成
2021年10月20日,Moderna在美国临床试验网站(ClinicalTrials.gov)登记了其巨细胞病毒(CMV)mRNA疫苗mRNA-1647在16-40岁女性健康受试者中的有效性、安全性和免疫原性III期临床研究。
根据ClinicalTrials.gov网站信息显示,该临床研究目前在持续进行中(最新更新日期2022年5月27日),该项研究计划招募6900例受试者,受试者将在第1天、第57天和第169天通过肌肉注射(IM)接种mRNA-1647疫苗。试验预计2023年1月29日完成。
巨细胞病毒(CMV)是一种常见的病原体,属于疱疹病毒家族。先天性巨细胞病毒感染由受感染的母亲将病毒传染给未出生的婴儿引起。在美国,巨细胞病毒是导致出生缺陷的主要传染原因,每年大约有2.5万名新生儿感染CMV,大约20%的受感染婴儿存在出生缺陷。目前还没有预防CMV感染的疫苗获批。
mRNA-1647使用与mRNA-1273和mRNA-1653(hMPV-PIV3病毒疫苗)相同的LNP,由于上市产品此前已经建立了一些临床和监管先例,一套完备的脂质制剂的识别、测试和生产体系对于加快mRNA-1647进入临床试验可能起着重要作用。
mRNA-1647在1期研究中作为冷冻液体制剂提供,但从2期研究开始已变更为冻干制剂,据报道冻干剂型的mRNA-1647在冷藏温度下可稳定18个月。
对比目前已上市两款新冠mRNA疫苗的有效期和储存条件,冻干剂型在提升制剂稳定性方面的作用可以说较为显著。
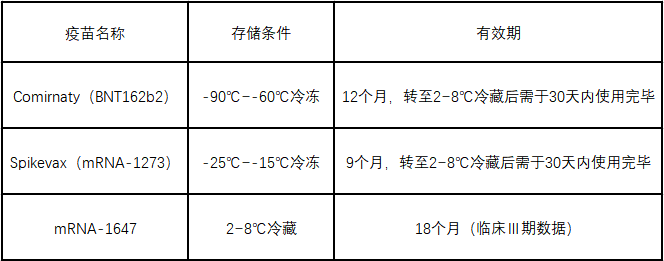
3.添加冻干保护剂可提升LNP稳定性
将制剂制成冻干粉是运输和长期储存许多药品的最常用方法之一。然而,冻干过程中结晶和真空脱水产生的应力可能会降低大分子或LNP的稳定性,导致生物活性丧失。据报道,添加适当的冷冻保护剂,如海藻糖、蔗糖和甘露醇,可以以特定配方的方式保持LNP的稳定性。辉瑞(Pfizer)已启动一项3期研究,以比较冻干BNT162b2制剂与其冷冻液体BNT162b2制剂的安全性和耐受性。
艾伟拓长期稳定供应注射级海藻糖、蔗糖、TRIS/TRIS-HCl、HEPES等生物保护剂与缓冲盐,针对mRNA客户的特殊需求,AVT相关保护剂和缓冲盐在独有的超低内毒素,超高纯度和符合各国药典标准基础上,满足DNase&RNase-Free的特点,更好的助力mRNA-LNP等生物制剂生产与中外申报!
目前AVT生物保护剂与缓冲盐系列此产品已同各大中型药企建立良好合作关系,相关产品通过SGS第三方审计,高品质的糖类和缓冲体系产品助力多个mRNA客户项目成功进入临床试验。
针对核酸递送保护剂的稳定性问题,可添加小编微信预约专场技术交流
 艾伟拓期待为核酸递送系统的稳定性发展贡献自己的一份力量!
艾伟拓期待为核酸递送系统的稳定性发展贡献自己的一份力量!