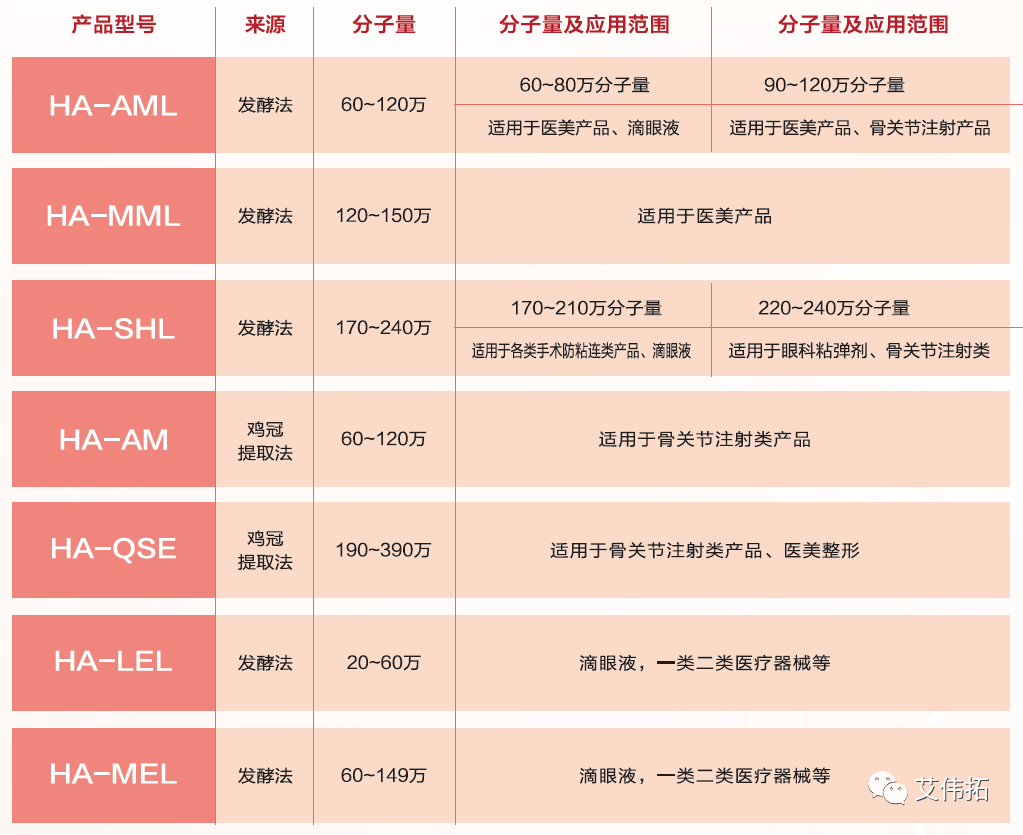
中国药典对透明质酸钠的原料质量有严格要求,包括蛋白质不超过0.1%、核酸不超过0.3%、内toxin不超过0.5EU/mg等参数。此外,微生物、重金属、乙醇含量等也是关注重点。水光类产品常使用发酵工艺生产的透明质酸钠,其中较大的技术难点在于控制内toxin残留。
严格控制透明质酸钠中的内toxin残留是非常重要的。内toxin通常是存在于革兰阴性菌外膜中的脂多糖,对宿主具有毒性。在细菌生长、繁殖、自溶或裂解的过程中,内toxin会从细菌外膜释放到周围环境中。当内toxin接触到皮肤中的巨噬细胞、中性粒细胞、内皮细胞、血小板等细胞时,会引发炎性反应和过敏反应,产生白细胞介素1、6、8、肿瘤坏死因子α、组胺、5-羟色胺、前列腺素、激肽等生物活性物质。这可能导致皮肤redness-and-swelling、疼痛、严重瘙痒、荨麻疹等炎症反应。
此外,内toxin还可能影响皮肤成纤维细胞的基因表达,促使正常成纤维细胞转化为增生性瘢痕成纤维细胞。因此,在选择透明质酸钠原料时,控制内toxin残留的原则是尽量低。
目前来说,中国药典对透明质酸钠内toxin的要求是低于0.5EU/mg,而日本丘比对内toxin残留的控制可以稳定在0.001 EU/mg以下,比药典标准低了整整500倍,也要比国内同类产品低了1~2个数量级,占据了absolute的优势。
艾伟拓长期稳定提供注射级透明质酸(CDE已登记),欢迎来询!